Контрольная
Вариант 6, контрольная 1. АГМУ
300.00 руб
Дата сдачи: Май 2012
1. Рассчитайте среднюю массу молекулы газа, 0,25 л (н.у.) которого имеют массу 0,1898 г.
2. При некоторой температуре в гомогенной системе
4HCl + О2 =2Сl2 + 2Н2О
установилось равновесие при следующих концентрациях:
[Cl2] = 0,1 моль/л; [HCl] = 0,25 моль/л; [О2] =0,2 моль/л. Рассчитайте концентрации исходных веществ в начальный момент.
3. Сколько мл воды нужно прибавить к 100 мл 50% (по массе) раствора азотной кислоты с плотностью 1,31 г/ мл, чтобы получить 20% (по массе) раствор?
4. Оцените реакцию среды (рН < 7, рН > 7, рН = 7) водных растворов следующих солей: дигидроарсената калия; сульфата аммония; ацетата лития. Напишите уравнения реакций в ионном и молекулярном виде.
5. 2 мл 72% (по массе) раствора азотной кислоты с плотностью 1,43 г/мл разбавили до 2 л. Найдите рН полученного раствора.
6. Одинакова ли будет окраска лакмуса при смешении растворов, содержащих в эквивалентных количествах:
а) аммиак и соляную кислоту;
б) гидроксид натрия и соляную кислоту;
в) гидроксид натрия и уксусную кислоту?
Напишите уравнения соответствующих реакций и дайте аргументированный ответ.
7. Назовите следующие комплексные соединения, определите степень окисления и координационное число комплексообразователя, дентатность лигандов:
[Co(NH3)4(NO3)Cl]Cl, Ca[Ru(H2O)(CN)5]2, [Pt(NH3)5OH]Br3. Напишите выражение для константы нестойкости по шестой ступени для комплексного соединения сульфата гексаамминиридия (III).
8. Сколько граммов металлического бария нужно взять, чтобы при его растворении в 1 л воды получить 4,92% (по массе) раствор гидроксида бария?
9. Валентные орбитали центральных атомов в молекулах метана, аммиака и воды имеют один тип гибридизации, хотя углы между связями не равны. Предложите пространственное строение молекул этих веществ и объясните различия в валентных углах, используя положения МВС.
10. Согласно принципу неопределенности:
• движение микрочастиц описывается определенной траекторией;
• невозможно точно определить местоположение микрочастицы и её импульс;
• возможно точно определить местолорожение микрочастицы и её импульс;
• движение микрочастицы можно рассматривать как волновой процесс.
11. При образовании иона BF4- донор электронной пары
• атом бора;
• ион бора;
• атом фтора;
• ион фтора;
• молекула BF3.
12. При уменьшении энергии активации химической реакции величина сопровождающего её теплового эффекта:
• уменьшается;
• увеличивается;
• не изменяется.
13. Растворимость кислорода в воде увеличивается при:
• понижении температуры;
• увеличении давления;
• повышении температуры;
• понижении давления;
• добавлении к воде хлорида натрия.
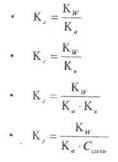
14. Константа равновесия для гидролиза соли по аниону имеет вид