Контрольная
Физическая и коллоидная химия Вариант 20 Контрольная работа № 1, АГМУ
Дата сдачи: Ноябрь 2010
1. В термодинамике теплота процесса считается положительной:
А. если получена системой от окружающей среды
Б. при переходе теплоты от системы к ее окружению
2. Если процесс изобарический, то:
а. P = const
б. ΔР = const
в. ΔН = ΔU + pΔV
г. Q = ΔН + рΔV
д. ΔH = Q
3. Если плавление льда происходит при постоянном давлении и температуре, а плотность льда меньше плотности воды, то:
а. А > 0
б. Q > 0
в. A < 0
г. Q < 0
4. При стандартных условиях равны нулю теплоты образования следующих веществ:
а. S(ромб)
б. Cl2
в. CO2
г. H2O
д. H2
5. Разность между СР и CV:
а. практически равна нулю для жидких и твердых тел
б. равна работе расширения при нагревании 1 моль газа на 1 К
в. практически равна нулю для веществ, находящихся в газообразном состоянии
г. достаточно велика и ее надо учитывать для газов
6. Теплота сгорания
7. Если процесс увеличивает энтропию изолированной системы, то:
а. прекращение всех процессов произойдет, когда энтропия системы достигнет минимального значения
б. установление устойчивого равновесного состояния произойдет. Когда энтропия достигнет максимального значения
в. прекращение всех процессов произойдет в состоянии равновесия
8. Объединенное уравнение первого и второго знаков термодинамики имеет вид:
а. TdS ≥ dU – pdV
б. TdS ≤ dU + pdV
в. dQ = dU + pdV
г. dS ≥ δQ/T
9. Так как энтропия представляет меру беспорядочности молекулярного состояния системы, то:
а. наличие примесей и дефектов в кристаллической решетке увеличивает энтропию
б. газообразному состоянию свойственно наибольшая энтропия
в. наличие примесей и дефектов в кристаллической решетке уменьшает энтропию
г. энтропия кристалла с идеальной кристаллической решеткой при абсолютном нуле равна нулю
10. Внутренняя энергия – это функция от переменных:
а. температуры
б. давления
в. объема
г. энтропии
д. энтальпии
11. Функция, равная «Н - ТS» - это
а. функция состояния
б. экстенсивное свойство систем
в. изобарно – изотермический потенциал
г. мера обесцененной части энергии
д. критерий вероятности самопроизвольных процессов при T, V = const в закрытых системах
12. Математически условия устойчивого равновесия в закрытой системе при P, S = const можно записать:
а. ΔU ≤ 0
б. ΔG = 0
в. ΔF = 0
г. ΔН = 0
д. S = max
13. Константа КР и КN связаны соотношением:
а. KP = KN · pΔn
б. KP = KN · p –Δn
в. KN= KP · pΔn
г. KP = KN · (RT/P)Δn
д. KP = KN · (P/RT)Δn
14. В случае гетерогенных реакций в выражение константы химического равновесия (КР) не вводят…
а. парциальные давления газообразных участников реакции
б. концентрации газообразных участников реакции
в. парциальные давления (или концентрации) веществ в твердом состоянии
г. парциальные давления (или концентрации) веществ в жидком состоянии
д. концентрации веществ, химические потенциалы которых постоянны
15. В уравнении изотермы химической реакции величины ΔG:
а. определяет работу перехода системы из данного состояния в равновесное
б. не определяет работу перехода из данного состояния в равновесное
16. Аналитический вид зависимости КХ от давления устанавливает уравнение (если Х – мольная доля)…
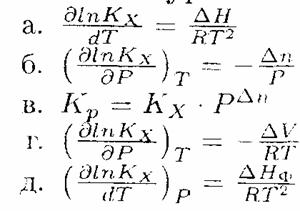
17. Общим термодинамическим условием фазового равновесия является:
а. равенство химических потенциалов каждого компонента во всех фазах системы
б. равенство нулю суммы химических потенциалов всех компонентов системы
в. равенство парциальных давлений насыщенного пара каждого компонента для всех фаз
18. На диаграмме состояния серы одновариантными, удовлетворяющими условию С = 1 – 2 + 2 = 1 являются…
а. одна система
б. две системы
в. три системы
г. пять систем
д. шесть систем
19. Из диаграммы состояния следует:
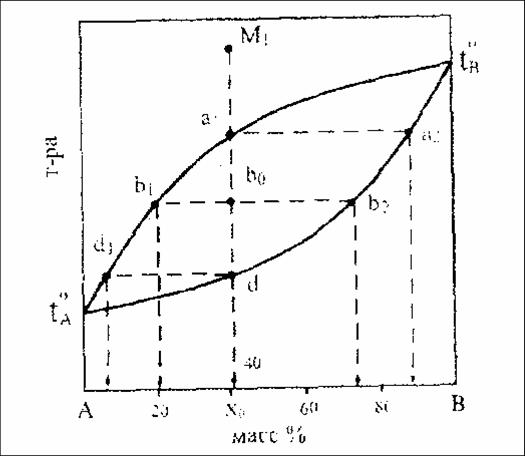
а. в процессе кристаллизации системы состава Х0, состав жидкой фазы изменяется от «а1» до «d1»
б. в конце кристаллизации системы, содержащей 40 масс % В, состав твердой фазы и исходной системы совпадают
в. в начале кристаллизации системы состава «Х0», первые кристаллы твердой фазы обогащены компонентом В по сравнению с исходной системой
г. при температуре «t2» исходная система трехфазна и, следовательно, инвариантна
д. последние капли жидкости, при завершении кристаллизации системы «Х0» имеют состав d1
20. На диаграмме состояния …
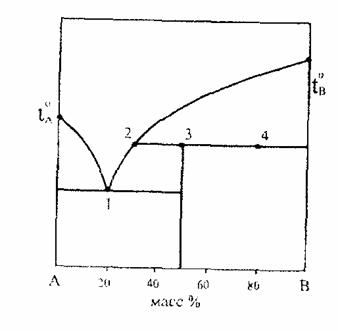
а. перетектический расплав содержит 30 масс % В
б. эвтектический расплав содержит 50 масс % А
в. перетектический расплав содержит 50 масс % А
г. химическое соединение содержит 50 масс % В, существует в твердом состоянии, так как плавится с разложением
д. система инвариантна в точках 1, 2, 3, 4
21. При расширении 110 г диоксида углерода от 50 до 175 л при 17º С совершается работа:
а. 15.5 · 102 Дж
б. 7550 Дж
в. 601 · 102 Дж
г. 7.55 кДж
22. Если разложение гремучей ртути происходит согласно уравнению Hg(CNO)2 → Hg + 2CO + N2 + 364,2 кДж/моль
а. 1279 кДж
б. 0,2361 м3
в. 6395 кДж
г. 1,181 м3
д. 0,7083 м3

