Контрольная
Барнаул Вариант 17 Контрольная работа 2
Дата сдачи: Сентябрь 2011
ЗАДАЧИ РЕШЕНЫ В ПИСЬМЕННОМ ВИДЕ, ПЕРЕВОД В ПЕЧАТНЫЙ ВИД НЕОБХОДИМО ОСУЩЕСТВЛЯТЬ САМОСТОЯТЕЛЬНО
1. Если при Р,Т = const массу всех компонентов раствора увеличить в два раза, то:
а. интеасввные свойства не изменятся
б. экстенсивные свойства возрастут в два раза
в. концентрация, малярный объем возрастут в два раза
г. общий объем, энтальпия, энтропия и теплоемкость возрастут в два раза
2. При равных концентрациях давление насыщенного пара всегда ...
а. больше над раствором летучего вещества по сравнению с раствором нелетучего
б. меньше над раствором летучего вещества по сравнению с раствором нелетучего
в. одинаково над раствором летучего и нелетучего растворенного вещества
3. При P,T = const термодинамическое условие самопроизвольного образования истинного раствора ...
а. ΔGсм = n1Δμ l + n2Δμ2 = 0
б. ΔGсм = n1Δμ l + n2Δμ2 > 0
в. ΔGсм = n1Δμ l + n2Δμ2 < 0
4. Буферным действием обладают:
а. растворы амфолитов
б. разбавленные растворы сильных кислот и щелочей
в. разбавленные растворы слабых кислот и щелочей
г. растворы солей слабых и средних многоосновных кислот
д. растворы слабой кислоты и ее соли и сильного основания
5. He относятся к буферным системам организма:
а. ацетатный буфер
б. бикарбонатный буфер
в. фосфатный буфер
г. гемоглобиновы буфер
д. оксигемоглобиновый буфер
6. Прп высокой концентрации компонентов в буфере буферная емкость максимальна, если:
а. рН < рКа
б. рOН < рКВ
в. рН = рКа
г. рН = рOH
д. рOН = рКB
7. Степень электролитической диссоциации одного и того же электролита, определенная различными методами, имеет:
а. одинаковое значение для слабых электролитов
б. разное значение для слабых электролитов
в. развое значение для сильных электролитов
г. одинаковое значение для сильных электролитов
8. Суммарной заряд ионной атмосферы ...
а. одинаков по знаку с центральным ионом
б. всегда с отрицательным знаком избыточного заряда
в. равен, но противоположен по знаку заряда центрального иона
г. равен по величине и одинаков по знаку заряда центрального иона
9. Эквивалентная электропроводность зависит от:
а. концентрации
б. температуры
в. вязкости раствора
г. скорости движения ионов
д. постоянной электрохимического сосуда
10. Если экспериментально определены изменения концентрации исходного вещества в зависимости от времени, то для определения константы скорости реакции 1-го порядка:
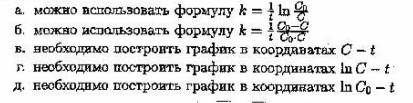
11. При выводе уравнения для константы скорости сложной химической реакции необходимо использовать:
а. закон действующих масс
б. принципы независимого течения реакций
в. принципы соответствия
г. принципы непрерывности
12. С повышением температуры:
а. скорость химической реакции увеличивается
б. константа скорости химической реакции увеличивается
в. температурный коэффициент γ увеличивается
г. константа скорости химической реакции не изменяется
д. температурный коэффициент γ уменьшается
13. Раздробленность дисперсной фазы характеризуют:
а. степенью дисперсности
б. удельной поверхностью
в. суммарной площадью границы раздела фаз, приходящейся аа единицу объема дисперсной фазы
14. Поверхностно-инактивными веществами являются:
а. глицерин
б. сахароза
в. этилацетат
г. сульфат магния
д. α-аминопентановая кислота
15. Коэффициенты в уравнении Фрейндлиха можно определить из графика зависимости:
а. С/Г = f(С)
б. Г = f(C)
в. lgГ = f(lgC)
г. σ = f(С)
д. Г/С = f(C)
16. В системе «полярный адсорбент - неполярный растворитель - ПАВ» молекулы адсорбтива:
а. обращеиы полярной частью к поверхности адсорбента
б. неполярной частью погружены в растворитель
в. обращевы гидрофильной частью к поверхности адсорбента
г. гидрофильной частью погружены в растворитель
д. обращены гидрофобной частью к поверхности адсорбента
17. Из уравнения ![]() следует что:
следует что:
а. масса диффундирующего вещества пропорциональна ско рости диффузии
б. масса диффундирующего вещества пропорциональна коэффициенту диффузии
в. поток диффузии пропорционален градиенту концентраций
г скорость диффузии пропорциональна времени течения процесса
д. скорость диффузии пропорциональна градиенту концентраций
18. Явление аддетивности присуще:
а. молярному коэффициенту поглощения
6. коэффициенту светораоссеяния
в. интенсивности светорассеяния
г. оптической плотности
д. экстинкуции
19. В полученном по реакции AgNO3 + NaCl(избыток) → золе быструю стадию явной коагуляции можно наблюдать, если ...
а. при добавления 0,1 Н раствора NaNO3 в пороговой концентрации значение злектрокинетического потенциала снижено до критического
б. при добавление избытка NaN03 схема мицелл в золе имеет вид - {m(АgС1)nСl- · (n -x)Na+}x- · xNa+
в. при добавлении избытка 0,1 Н раствора NaNO3 строение мицелл в золе имеет вид - {m(АgС1)nС1- • nNa+}
г. при добавлении избытка система находится в изоэлектрическом состоянии
20. Понятие росклинивающее давлениеиспользуется в теории ...э
а. коагуляции Г. Фрейдлиха
б. коагуляции Г. Мюллера
в. устойчивости гидрофобных дисперсных систем ДЛФО
21. Если для приготовления 3л ацетатного буфера с рН = 5,24 (рК = 4.76) использованы сантимолярные растворы соли и кислоты, то в буфере содержится:
а. 0,0225 моль соли
б. 0,0075 моль кислоты
в. 0,0125 моль соли
г. 0,225 моль кислоты
д. 0,075 моль кислоты
22. В реакции 2А2(г) +В2(г) ↔ 2А2В(г) при уменьшении вещества A2 в 4 раза скорость прямой реакции не изменится, если концентрацию вещества В2 увеличить в:
а. 2 раза
б. 4 раза
в. 8 раз
г. 16раз
д. 12 раз

