Контрольная
Барнаул Вариант 19 Контрольная работа 2
Дата сдачи: Август 2011
ЗАДАЧИ РЕШЕНЫ В ПИСЬМЕННОМ ВИДЕ, ПЕРЕВОД В ПЕЧАТНЫЙ ВИД НЕОБХОДИМО ОСУЩЕСТВЛЯТЬ САМОСТОЯТЕЛЬНО
Решения на 20 задачу нет
1. Зависимость давления насыщенного пара компонента над раствором от его концентрации в растворе описывается
а. законом Дальтона в случае идеальных систем
б. законом Рауля в случае идеальных систем
в. Законом Вант – Гоффа
г. Законом Генри для растворенного вещества в случае предельно разбавленного раствора.
2. Молярные объем, внутренняя энергия и изохорно – изотермический потенциал индивидуальных веществ, и соответствующие им парциальные молярные величины компонентов совершенного бинарного раствора находятся в соотношении:
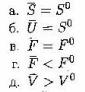
3. Относительное понижение температуры замерзания – это:
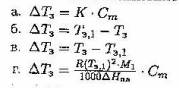
4. Буферные системы классифицируют на:
а. буферные системы организма.
б. минеральные
в. Биологические
г. люминисцентные
д. кислотные5. рН фосфатной буферной системы увеличится при добавлении к ней:
а. воды
б. гидроксида натрия
в. соляной кислоты
г. дигидрофосфата натрия
д. гидрофосфата натрия
6. Буферная система более устойчива к добавлению щелочи, если …
а. рН = рКа + 1
б. рН = рКа – 1
7. Электростатическая теория сильных электролитов предложена…
а. С. Аррениусом
б. П. Дебаем
в. Гюккелем
г. В. Освальдом
д. Н. А. Измайловым
8. Уравнение, связывающее среднюю ионную активность «а±» электролита СuBr2 с активностью этого электролита «а» имеет вид:
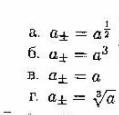
9. Удельная электропроводноять водных растворов сильных электролитов при высоких концентрациях …
а. уменьшается, так как вместе с ростом числа ионов уменьшается скорость их движения
б. уменьшается, так как понижается степень диссоциации электролита
в. Возрастает, так как увеличиваются числа переноса
10. Укажите оси координат, в которых для реакции первого порядка зависимости носят линейный характер:
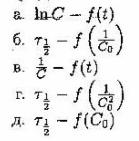
11. В последовательной реакции ![]() максимальный выход промежуточного вещества возможен, если:
максимальный выход промежуточного вещества возможен, если:
а. первая стадия процесса – лимитирующая
б. вторая стадия процесса – лимитирующая
в. первая стадия процесса – главная
г. вторая стадия процесса – главная
12. Правило Вант – Гоффа математически можно записать:
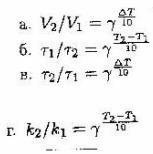
13. Удельная поверхность частиц кубической формы объемом 1 см3 равна:
а. 6 см-1
б. 6 см2
в. 6 · 102 м-1
г. 3 · 10-2 м-1
д. 6 · 10-2 м2
14. Поверхностная активность – это…
а. величина, характеризующая удельную адсорбцию
б. способность растворенных веществ изменять поверхностное натяжение
в. величина, связанная с удельной поверхностью15. Поверхностное натяжение на границе «жидкость - газ» - с увеличением давления:
а. повышается
б. понижается
в. практически не зависит от давления
16. Адсорбция электролитов – это …
а. химический процесс
б. хемосорбция
в. физический процесс
г. физическая адсорбция
17. Уравнение Релея позволяет количественно охарактеризовать интенсивность светорассеяния света в золях, если:
а. это золи неметаллов
б. это золи металлов
в. размеры частиц золя не превышают половину длины волны падающего светового потока
г. не изменяется степень дисперсности
д. система оптически однородна
18. Электронейтральны:
а. гранулы
б. агрегаты
в. собственно коллоидные частицы
г. мицеллы
д. образования состоящие из гранул, диффузного слоя противоионов и дисперсионной среды
19. Положительное привыкание золей наблюдается при:
а. добавления электролита коагулятора отдельными порциями
б. одновременном добавлении электролита коагулятора
в. добавлением незначительных количеств ВМС
д. коалеценции
20. НЕТ
21. Для приготовления 1л 0.1 М ацетатного буфера с рН = 5.24 (рКа = 4.76) необходимы объемы децимолярных растворов кислоты и соли:
а. Vсоли = 250 мл; Vк-ты = 750 мл
б. Vсоли = 750 мл; Vк-ты = 250 мл
в. Vсоли = Vк-ты = 500 мл
г. Vсоли = 225 мл; Vк-ты = 775 мл
д. Vсоли = 820 мл; Vк-ты = 180 мл
22. Если в некоторой реакции при изменении начальной концентрации от 1 до 3 моль/л период полураспада уменьшается с 3 ч до 20 мин, то порядок реакции:
а. нулевой
б. первый
в. второй
г. третий

